Grundlogn vo da Chemie
De Chemie is de Natuawissnschoft, de wos si mim Aufbau, mit de Eignschoftn und de Reaktiaunan vo Stoffn bschäftigt. Stoffe san Materie und bestehngan aus Atoman, Moleküün, Nanopartikln, Cluster, ...
Eitäulung vo de Stoffe
[Werkeln | Am Gwëntext werkeln]- Reinstoffe:
- Elemente: bestehngan aus ana anzlnan Suatn vo Atoman, z. B.: Fe, O2
- Vabindungan: aus vaschiedanan Atoman in definiatn Menganvahöötnissn (Moleküin), z. B.: H2O, NaCl
- Gemische/Gemenge:
- Homogen: schaun aus wiara Reinstoff, san owa molekuloa dispers glöst (Täuchen kloana 1 nm), z. B.: Soizlösungan, maunche Legierungan
- Kolloide und Nanopartikl: kolloidal glöst (Täuchen 1 nm bis 1 μm), z. B.: Dispersionsfoabn, Zementsuspensiaun
- Heterogen (= Dispersionan): vaschiedane Phasn san nemaranaund vamischt (grob dispers vatäut, Täuchen gressa 1 μm), z. B.: Granit, PU-Schaum.
Bezeichnungan fia Gemische, nachm Aggregatszuastaund: (rot = homogen, gööb = heterogen):
| fest | flüssig | gasfeamig | |
| in fest | Legiarung, wia Bronze | Tonminaroi | laara Schwaum, Hoatschaum |
| Gemenge i.e.S., wia Granit | |||
| Haufweak, wia Kias | |||
| in flüssig | Lösung, wia Sole | Lösung, wia Weih | Lösung, wia Sodawossa |
| Suspension, wia Schlaum | Emulsion, wia Müli | Schaum | |
| in gasfeamig | Aerosol (Obabegriff) | Gasgmisch | |
| Rauch, Staub, wia Tschickrauch | Daumpf, Nebl | ||
Chemische Elemente
[Werkeln | Am Gwëntext werkeln]Mittlawäu kennan mia 118 vaschiedane Elemente, 91 davo kumman in da Natua vua. A jeds Atom (griech. atomos „untäuboa“) hod an kloan positiv glodanan Kean (dea bsteht aus positiv glodanan Protonan und neutroin Neutronan) und ane Hüün aus negativ glodanan Elektronen. A noch außn unglodans Atom muass glei vü Protonan wia Elektronan haum. A Atom mit da sööm Protonanauzoi (Uadnungszoi) kau vaschiedn vü Neutronan haum, des san de Isotope (lat. ísos „gleich“ und tópos „Ort, Stelle“). Instabüle Isotope vafoin noch ana gwissn Zeit, des is de Hoibweatszeit (Zeit, wo de Hööftn vo de Atome in aundare Elemente zafoin is), dabei wiad radioaktive Strohlung ausgstoid (das haßt owa ned, dass olle Isotope radioaktiv san).
A poa Begriffe:
- Massnzoi (MZ): is de Summan (vo de Massn) vo de Neutronan und Protonan. Untaschiedliche Isotope vom sööm Element reagian chemisch gleich, z. B. H2O, HOD, D2O, T2O (H = Wossastoff, D = Deuterium, T = Tritium - Wossa, hoibschwars Wossa, schwars Wossa, Iwaschwars Wossa)
- Obsolute Atommassn: is de Massn vo an Atom in g oda kg, z. B. 1 Atom 12C hod de Massn vo ca. 2 · 10−23 g.
- Relatiave Atommassn: wiad in da Atomarn Massneiheit u auge'm. 1 u is 1/12 vo da Massn vo an Atom vom Isotop 12C = 1,66053892 · 10−24 g.
- Relatiave Moleküümassn: is de Summan vo oin relatiavn Atommassn vo oin Atoman vo an Moleküü.
Bohrsches Atommodöö
[Werkeln | Am Gwëntext werkeln]
De Elektronen san auf anzelne kraasfeamige Schoin rund uman Kean auftäut (K = 2e, L = 8e, M = 8e, N = 18e, …). De aißaste Schoin bstimmt de Eignschoftn vo dem Element. A jeds Atom schaut, dass a volle Außnschoin kriagt, drum gehts Bindungan ei. Außa de Edelgase, de haum scho a volle Außnschoin, drum san de ned seah reaktiv.
Orbitalmodöö
[Werkeln | Am Gwëntext werkeln]
In Wirklikeit schauts a wengl aundas aus. De Elektronen kaunst nämli ois Wöön oda Täuchen betrochtn (Welle-Täuchen-Dualismus). Durch Iwalogerung vo de Wöönfunktionan kriagt ma Bereich', wo se de Elektronan mit ana eahähtn Woahscheinlikeit aufhoidn, des san de Orbitale.
Periodnsystem
[Werkeln | Am Gwëntext werkeln]
Es Periodnsystem vo de Elemente (PSE) is 1869 vom Dmitri Mendelejew und vom Lothar Meyer unohhängig voranaund entwicklt wuan (aufbauend auf ihm J. A. R. Newland sein „Gsetz vo de Oktave“). De Elemente mit de gleichn Eignschoftn stehngan untaranaund in da sööm Gruppn; noch aufsteigenda Massn (MZ) greiht. Domois hods aa no Lückn gem, wo ma scho de Eignschoftn vo de no unentdecktn Elemente im Vuahinein hod sogn kinna (1875: Gallium, 1879: Scandium, 1886: Germanium - de kumman in da Natua vua). Späda hod ma no einige Elemente künstli heagstööt, owa de san noch wenign Millisekundn wieda zafoin. De meistn Elemente san bei Raumtemperatua und Noamäudruck fest und metollisch. Brom und Quecksüwa san flüssig, Wossastoff, Stickstoff, Sauastoff, Fluor, Chlor und de Edlgase san gasfeamig.
- 1. HG: Alkalimetolle (+ Wossastoff)
- 2. HG: Erdalkalimetolle
- 3. HG: Borgruppm
- 4. HG: Kuinstoff-Silicium-Gruppm
- 5. HG: Stickstoff-Phosphor-Gruppm
- 6. HG: Chalkogene
- 7. HG: Halogene
- 8. HG: Edlgase
De Atommassn steigt vo obm noch untn und vo links noch rechts. Da Atomradius nimmt vo obm noch untn zua, vo links noch rechts oh (bei de Hauptgruppn, wäu sa se stärka auziahn). De Elektronegativität (des is de Fähigkeit vo an Atom, dass Bindungselektronan aun si zaht) nimmt vo obm noch untn oh und vo links noch rechts zua. De Ionisiarungsenergie (oiso de nötiche Energie, ums am schwächstn bundane Elektron vo an Atom zan entfeanan) nimmt vo obm noch untn oh und vo links noch rechts zua (Ausnauhm: Edlgase).
Chemische Vabindungan
[Werkeln | Am Gwëntext werkeln]Chemische Vabindungan bstengan aus Atoman in definiatn Menganvahöötnissn, de wos mitaranaund vabundn san; des kennan sei: Moleküü, Ionangitta, Metoigitta, Komplexe oda Cluster. De Summanfuaml gibt de Auzoi vo jeda Atomoat im Moleküü oda in ana Fuamleiheit au, z. B.: C6H6, C60, NaCl, C37H67NO13. De Struktuafuaml zoagt de Vaknüpfungen vo de Atome schematisch.
Ma untascheidt organische Vabindungan (devventhoidn Kuinstoff und Wossastoff) und aunorganische. Da Kuinstoff kau via Bindungan eigeh; ois irdische Lem basiat aufm Kuinstoff. Fricha hod ma glaubt, nua's Lem kau organische Stoffe produzian („vis vitalis“), owa jeda Natastoff (aa unsare DNA) kau synthetisch heagstööt wean, waunst genau waßt, wia's zaumgsetzt is, wäu ois aus den sööm Atoman bsteht. Ois easchtas hod da Wöhler organische Substanz aus aunorganischn Ausgaungsstoffn heasgööt (1824: Oxalsäure duach Hydrolyse vo Dicyan; 1828: Harnstoff aus Ammoniumcyanat).
De Oxidationszoi (Oxidationsstufn, elektrochemische Weatigkeit): gibt de Ionanlodung vo an Atom in ana chemischn Vabindung oda in an mehratomign Ion au, desd hädast, waun de Vabindung nua aus oaatomign Ionan bstengan ded. In ana lodungsneitroin Vabindung is de Summan vo de Oxidationszoin 0. Domitsd des ned mit de Ladungan vawexlst, schreibt ma de Oxidationszoi noamalaweis mit römischn Ziffan, z. B.: H2O = H+I2O-II, FeO = Fe+IIO-II, Fe2O3 = Fe+III2O-II3.
Ionanbindung
[Werkeln | Am Gwëntext werkeln]
Meist is fiara Atom (energetisch) gscheida, dass a Bindung eigeht ois wia dass aloa existiat (bei Menschn is nix aundas). Des elektronegativare Element nimmt Elektronan vom elektropositivarn auf, des haßt, beide Atomsortn liagn nocha ionisiat vua. De Kationan (positiv glodn) und Aunionan (negativ glodn) übn a ungrichte elektrostatische Aunziachung (Kationan-Aunionan) bzw. Ohstoßung (Kationan-Kationan, Aunionan-Aunionan) aus. Des fiaht zua Ionankristoin mit ana periodischn Aunuadnung vo de Kationan und Aunionan, des san Soize wia z. B. NaCl. Ionankristoi san spröd, wäu se de gleich glodanan Ionan bei ana Vaschiabung ohstoßn.
Metoibindung
[Werkeln | Am Gwëntext werkeln]
A Metoi hod a kloane Elektronanaffinität (EA). In an Metoigitta gem de Metoiatome eahna aißan Elektronan oh, de wos daun ois „Elektronangas“ delokalisiat zwischn de vabliabanan, positiav glodanan Atomrümpfn vualiagn. De Atomrümpf' uadnan se periodisch in an Metoigitta au; es Elektronangas hööts zaum und steht fia de Leitung vo elektrischm Strom zua Vafügung. Metoi san im Untaschiad zua an Ionankristoi guad vafuamboa.
Atombindung (kovalente Bindung)
[Werkeln | Am Gwëntext werkeln]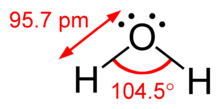
Maunche Atome kennan se Elektronan täun, wauns a gmeinsaums Moleküüorbitoi duach Iwaloppung vo eahnare Atomorbitole büdn. De Bindung is raimlich gricht'; de Bindungslängan und da Bindungswingl kennan gmessn wean. De Atombindung kau apolar (bei gleichn Partnan) oda polar sei.
Wossastoffbrücknbindungan
[Werkeln | Am Gwëntext werkeln]Wossa is a polare, kovalente Vabindung. Da Sauerstoff is elektronegativa ois wia da Wossastoff, drum ziahgt a de Bindungselektronan stärka aun si. Des fiaht zua positiavn Partiäulodungan aum Wossastoffatom und zua negatiavn am Sauerstoff (Dipol). Drum kriagst schwoche elektrostatische Wechslwiakungen zwischn de Moleküü, des is a da Grund, warums Wossa so an hochn Siedepunkt hod (zan Vagleich H2S: -60 °C, CH4: -160 °C). Meak da: De Atombindung söwa wiakt innahoib vo an Moleküü, de Wossastoffbrücknbindungan wiakn zwischn zwoa Moleküün.
Chemische Reaktionen
[Werkeln | Am Gwëntext werkeln]Massneahoitungsgsetz
[Werkeln | Am Gwëntext werkeln]Es Massneahoitungsgsetz is 1758 vom Lavoisier aufgstööt wuan: „Die Summe der Massen der Edukte (Ausgangsstoffe) ist immer gleich der Summe der Massen der Produkte (Endstoffe).“ Des haßt, bei chemischn Reaktionsgleichungan muass auf da linkn Seitn de de söwe Auzoi vo jeda Atomsortn stehn wia auf da rechtn. In da Physik güüt des ned (Keanspoitung, Keanfusion).
Gsetz vo de konstauntn Propoationan
[Werkeln | Am Gwëntext werkeln]Es Gsetz vo de konstauntn Propoationen is 1797 vom Proust aufgstööt wuan: „Das Massenverhältnis der Elemente in einer definierten Verbindung ist immer konstant.“ Eh kloa, wäu aa's Vahöötnis vo de Atome in ana Vabindung konstant is. Beispü: Es Vahöötnis vo Na zu Cl in NaCl ist imma 23:35,5; es Vahöötnis vo Ca zu O in CaCO3 is imma 40:48 [rel. Atommassen in u: Na (23); Cl (35,5); Ca (40); O (16)].
Stoffmengan
[Werkeln | Am Gwëntext werkeln]De Stoffmengan n is a Moß fia de Auzoi vo Täuchen. De Eiheit vo da Stoffmengan is Mol. 1 mol san 6,023 · 1023 Täuchen, des san genauso vü, wia 12 g vom Isotop 12C. De Massn m vo an Mol aun gleichn Täuchen is de Molare Massn M (Molmassn). M = m/n.
- Beispü CO2: Wia vü wiagt oa Mol CO2? Wia vü g Sauastoff und wia vü g Kuinstoff enthööt oa Mol CO2?
- 1 mol CO2 enthööt 6,023 · 1023 CO2 Moleküü. 1 mol CO2 enthööt 6,023 · 1023 C-Atome. 1 mol CO2 enthööt 2 · 6,023 · 1023 O-Atome.
- Ausm PSE kriagt ma de Molmassn vom O: 16 g/mol und vom C: 12 g/mol. Draus rechnast da de Molmassn vom CO2 aus: 12 + 2 · 16 = 44 g/mol.
- 1 mol CO2 enthööt 44 g CO2. 1 mol CO2 enthööt 1 mol C, des san 12 g C. 1 mol CO2 enthööt 2 mol O, des san (2 · 16) = 32 g O.
- Beispü Brennan und Leschn vo Koik:
- Koikbrennan: CaCO3 → CaO + CO2
- Leschen vo Brauntkoik: CaO + H2O → Ca(OH)2
- Wiavü kg CO2 entstehn beim Brennan vo 500 kg Koik?
- Wiavü Wossa vabraucht da dobei entstehende Brauntkalk theoretisch beim Leschn?
- Relatiave Atommassn (ausm PSE): Ca = 40 u; O = 16 u; C = 12 u; H = 1 u. Draus brechnast da de Molmassn: M(CaCO3) = 100 g/mol; M(CO2) = 44 g/mol; M(CaO) = 56 g/mol; M(H2O) = 18 g/mol
- 1 mol CaCO3 liafat da 1 mol CO2 → aus 100 g CaCO3 kriagst 44 g CO2 und aus 500 kg CaCO3 kriagst 220 kg CO2
- 1 mol CaCO3 liafat da 1 mol CaO, des 1 mol H2O bindt; aus 100 g CaCO3 büdn se 56 g CaO, des wos 18 g H2O bindt → aus 500 kg CaCO3 büdn se 280 kg CaO, des wos 90 kg H2O bindt.
Chemischs Rechnan wia des wos ma grod gmocht haum, nennt ma Stöchiometrie.
Massnwiakungsgsetz
[Werkeln | Am Gwëntext werkeln]Jede chemische Reaktion kaunst ois Gleichgeicht betrochtn, des Gleichgewicht kau owa seah untaschiadli liegn. Z. B.: Ioddaumpf (I2) und Wossastoff (H2) san in an Glaskuibn eigschlossn und reagian duach Zaumstessn zua Iodwossastoff (2 · HI). Waun gnua HI büdt wuan is, stessn aa HI-Moleküü zaum und wean wieda I2 und H2 büdn. Wo dass des Gleichgwicht liagt, wiad duachs Massnwiakungsgsetz bschriam:
mit:
- K ... Gleichgwichtskonstauntn (hängt oh vo da Temperatua)
- [i] ... Konzentration vom jeweilign Stoff [mol/l]
Bei schwaalöslichn Stoffn haßt de Gleichgewichtskonstauntn Löslichkeitsprodukt KLP.
A Spezialfoi san de oszilliarandn Reaktionan, des is a System wos ohwechslnd hi- und zruck reagiat, z. B.: de „Iod-Uhr“ (Briggs-Rauscher-Reaktion: KIO3/H2SO4 + Malonsaire/MnSO4/Stärke + H2O2) oda de Taktgebung vo unsam Heazschlog (Sinusknotn).
Prinzip vom kloanstn Zwaung
[Werkeln | Am Gwëntext werkeln]Le Chatelier (1884): „Übt man auf ein chemisches System im Gleichgewicht einen Zwang aus, so reagiert es so, dass die Wirkung des Zwanges minimal wird.“ z. B.: Ammoniaksynthese 3𝐻2 + 𝑁2 ↔ 2𝑁𝐻3: Aus via Gasmoleküün wean zwoa – a Druckeahähung begünstigt de Reaktion.
Thermodynamik
[Werkeln | Am Gwëntext werkeln]De Thermodynamik sogt uns, ob a Reaktion iwahaupt owerennan kau.
- Enthalpie (Wärmetönung) H [J]: gibt ihn Energieumsotz vo ana chemischn Reaktion au. Dobei wiads imma vo da Seitn vom System augschaut, des haßt, ΔH is negatiav bei ana Energieohgobm aun de Umgebung; z. B. de Schmöözenthalpie is de Wärmemengan, dest brauchst, um an Feststoff zan schmöözn.
- Entropie S [J/K]: is de statistische Zoi vo de meglichn, energetisch gleichweatign Mikrozuaständ' vo an System. A System, des wos si söwa iwalossn is, kriagt a Maximum vo Entropie, wäu des aum woahscheinlichstn is.
De Fundamentoigleichung vo da Thermodynamik lautet:
Domit a chemische Reaktion owerennt, muass' exergon sei, des haßt, de freie Enthalpie G muass ohnehma.
mit:
- G ... freie Enthalpie [J]
- H ... Enthalpie [J]
- T ... Temperatua [K]
- S ... Entropie [J/K]
- Exotherme Reaktionan: ΔH is negatiav, des haßt, Energie (Wärme) wiad freigsetzt. Dabei kennan se hochg'uadnate Struktuan (niedrige Entropie) büdn, z. B. Fällungan/Kristallisationan.
- Endotherme Reaktionan: ΔH is positiav, des haßt, Energie (Wärme) wiad aus da Umgebung aufgnomman, dabei muass de Entropie zuanehma, z. B. gasfeamige Reaktionsprodukte.
De Entropie nimmt mit da Temperatua zua, drum findn entropiebstimmte Reaktionan wia a Zafoi bei hechan Temparatuan statt und energiebstimmte Reaktionan wiara Kristillation bei ana tiafan.
Kinetik
[Werkeln | Am Gwëntext werkeln]De Kinetik sogt uns, wia schnö dass a Reaktion owerennt. De Gschwindigkeit vo ana Reaktion, bis se's Gleichgwicht eistööt, kau duach de Temperatua erhäht wean. Wäu waun de Moleküü schnölla schwingan, stessns efta mitaranaund zaum. Ois Faustregl kaunst heanehma: Eahehung um 10° is a Vadoppelung vo da Reaktionsgschwindigkeit.
- [A] ... Konzentration vom Stoff A
- t ... Zeit
- k ... Gschwindigkeitskonstauntn (Arrhenius-Gleichung)
- A ... Frequenzfaktoa
- EA ... Aktiviarungsenergie
- R ... oigmoane Gaskonstauntn
- T ... Temperatua
Owa aa waunst de Konzentration, ihn Druck oda de Owaflächn eahehst, kaunst de Reaktion bschleinign.
Katalysatoan
[Werkeln | Am Gwëntext werkeln]„Ein Katalysator ist ein Stoff, der die Geschwindigkeit einer chemischen Reaktion erhöht, ohne selbst dabei verbraucht zu werden und ohne die endgültige Lage des thermodynamischen Gleichgewichts dieser Reaktion zu verändern.“ —Wilhelm Ostwald
De freie Enthalpie ΔG nimmt während da Reaktion oh. Domit de Reaktion iwahaupt auhebt, muass easchta de Aktiviarungsenergie EA aufbrocht wean. Waun EA hecha is ois wia de Energie, de wos zua Vafügung steht (Wärme, Strohlung, …), nocha kauns ned owerenna. Beispü: Schwoazpuiva – ohne Zündung gibts koa Reaktion ned. Katalysatoan setzn de Aktiviarungsenergie owe, drum kennans de Reaktion stoak bschleinign. Es wiad nua de Reaktionskinetik, owa ned de Thermodynamik vaändat; de Gleichgwichtskonstauntn K bleibt unvaändat.
Sairn und Basn
[Werkeln | Am Gwëntext werkeln]Sairn san Stoffe, de wos Wossastoffionan (H+, Protonen) aun an Reaktionspartna ohgem kennan (Protonandonatoren). Basn (Laugn) san Stoffe, de wos Wossastoffionan aufnehman kenna (Protonanakzeptoren). Wossa kau ois a Protonandonator wia aa ois Protonanakzeptor wiakn, des haßt, es is amphoter. In wässrign Lösungan liagn solvatisiate (glöste) Protonan ois Oxoniumion (H3O+) vua. Es Wossa reagiat ständig mit se söwa (Autoprotolyse), es dissoziiert täuweis zua Hydroxidionan (OH-) und Oxoniumionan (H3O+):
- 2 𝐻2𝑂 ↔ 𝐻3𝑂+ + 𝑂𝐻−
A Saire kau nua daun ois a Saire wiakn, waun a Basn zua Reaktion zua Vafügung steht (und umkeaht). In wässrign Lösungan steht's Wossa imma ois Reaktionspartna zua Vafügung, es reagiat beim Kontakt mit ana Sairn ois Basn oda beim Kontakt mit ana Basn ois Sairn. Beispü:
- 𝐻𝐶𝑙 + 𝐻2𝑂 ↔ 𝐻3𝑂+ + 𝐶𝑙−
- Chlorwossastoff + Wossa ↔ Oxoniumion + Chloridion
- 𝑁𝐻3 + 𝐻2𝑂 ↔ 𝑁𝐻4+ + 𝑂𝐻−
- Ammoniak + Wossa ↔ Ammoniumion + Hydroxidion
Wiast siechst, reagiat da Chlorwossastoff eascht nochm Kontakt mim Wossa (oda ana aundan Basn) ois a Saire bzw. da Ammoniak reagiat eascht im Kontakt mim Wossa (oda ana aundan Saire) ois Basn. De Lösung vom Chlorwossastoff HCl (des is a Gas) im Wossa is de Soizsaire, de vom Ammoniak NH3 (aa a Gas) im Wossa Ammoniumhydroxid (oda Ammoniakwossa, Salmiakgeist).
Soize
[Werkeln | Am Gwëntext werkeln]Reaktionsprodukte vo ana Sairn-Basn-Reaktion nennt ma Soize. Se bestehngan imma aus an negatiavn Anion (vo da Sairn) und am positiavn Kation (vo da Basn). Soize wean noch da zugrundeliagandn Sairn benaunt.
Z. B. de Soizsäure HCl reagiat mit da Basn Calciumhydroxid (Koikmüli) Ca(OH)2, des eagibt es Soiz Calciumchlorid CaCl2.
Sairestärkn und Basnstärkn
[Werkeln | Am Gwëntext werkeln]Irdndwaun stööt se a Gleichgwicht ei zwischn da linkn (z. B. HCl + H2O) und da rechtn Seitn (z. B. H3O+ + Cl-). Je weida rechts dass es Gleichgwicht liagt (des haßt, waun meah H3O+ büdt wiad), umso stärka is de Sairn. De Dissoziationskonstauntn vo da Sairn rechnast da mim Massnwiakungsgsetz aus, des is de Konzentration vo de Produkte duach de Konzentration vo de Edukte:
De Sairestärkn pKS is da negatiave dekadische Logarithmus vo da Dissoziationskonstantn (ihn Logarithmus kennma eh scho vom Schoi).
Dessöwe güüt a fia Basn:
und
pH-Weat
[Werkeln | Am Gwëntext werkeln]In reinam Wossa is imma a Gleichgwicht zwischn dissoziiatn Moleküün und undissoziiatn:
- 2 𝐻2𝑂 ↔ 𝐻3𝑂+ + 𝑂𝐻− (Autoprotolyse)
Mim Massnwiakungsgsetz kennan ma uns de Gleichgwichtskonstauntn ausrechna.
Wäu se de Konzentration vom H2O bei gleicha Temperatua ned wirkli ändat, kaunst des fire ziahn und so kriagst es Ionenprodukt vom Wossa:
- bei 0 °C: Kw = 0,1 · 10−14 (pKw = 14,939 = pH + pOH)
- bei 25 °C: Kw = 1,0 · 10−14 (pKw = 13,996)
- bei 60 °C: Kw = 9,6 · 10−14 (pKw=13,017)
Da pH-Weat (pondus hydrogenii) [dimensionslos] is da negative dekadische Logarithmus vo da Konzentration vo de Oxoniumionan [mol/l], da pOH-Weat is da negative dekadische Logarithmus vo da Konzentration vo de Hydroxidionan. Gaunz genau gnumma, is da pH-Weat da negative dekadische Logarithmus vo da Wossastoffionan-Aktivität.
z. B.: Da pH-Weat 0 haßt 1 mol H3O+ pro Lita und 0,00000000000001 mol OH- pro Lita, des entspricht an pOH-Weat vo 14. A pH-Weat vo 7 haßt neutroi, ois drunta is saua, ois driwa basisch (beim pOH-Weat is umkeaht).
Berechnung vom pH-Weat
[Werkeln | Am Gwëntext werkeln]Waun de Sairnstärkn bzw. Basnstärkn und de Konzentration bekaunt san, kaunst da ihn pH-Weat iwa de fuigendn Zaumanhäng' (näharungsweis) ausrechna.
- Massenwiakungsgsetz:
- Ionenprodukt vom Wossa:
- Massneahoitungssotz:
- Lodungseahoitungssotz:
Fia vaschiadn stoake Sairn hosd vaschiadene Fuamln:
- Gaunz stoake Sairn (pKS < 1):
- Stoake Sairn (1 < pKS < 4,5):
- Schwoche Sairn (4,5 < pKS < 9):
- Gaunz schwoche Sairn (Kw ≈ KS ∙ c0):
c(A) = [A] ... Konzentration vom Stoff A [mol/l]
Fia Basn vawendst de sööm Fuamln, nua stott H3O+ setzt OH- ei, und stottm KS nimmst des KB.
Neutralisation
[Werkeln | Am Gwëntext werkeln]Waun a Saire mit ana Basn vuiständig zua Soiz und Wossa reagiat, des a Neutralisation, de is stoak exotherm. Z. B. fia de Neutralisation vo 1 mol Schweflsaire (H2SO4) brauchst 2 mol Natriumhydroxid (NaOH).
Puffa
[Werkeln | Am Gwëntext werkeln]
Puffa san Stoffe, zu denansd a Saire oda Basn dazuagem kaunst, ohne dass se da pH-Weat groß vaändat, z. B. Essigsaire (HAc, CH3COOH) und Natriumacetat (NaAc, CH3COONa); es Dissoziationsgleichgewicht is:
- 𝐻𝐴𝑐 + 𝐻2𝑂 ↔ 𝐴𝑐− + 𝐻3𝑂+
Wauns Soiz vuiständig dissoziiat is, nocha kriagst: [NaAc] = [Ac-], waunst a wengl H3O+ - oda OH− dazuagibst, ändert se zwoa es [HAc] bzw. [Ac-] owa ned es [H3O+], des haßt, da pH-Weat bleibt relatiav konstaunt.
Schau aa
[Werkeln | Am Gwëntext werkeln]Literatua
[Werkeln | Am Gwëntext werkeln]- Charles E. Mortimer: Chemie – Das Basiswissen der Chemie. Thieme, Stuttgart 2003, ISBN 3-13-484308-0.
- Joachim Kranz, Manfred Kuballa: Chemie im Alltag. Cornelsen Scriptor, Berlin 2003, ISBN 3-589-21692-1.
- Pedro Cintas: Der Weg zu chemischen Namen und Eponymen: Entdeckung, Priorität und Würdigung. In: Angewandte Chemie. 116(44) (2004), S. 6012–6018, doi:10.1002/ange.200330074.
Im Netz
[Werkeln | Am Gwëntext werkeln]| Wikibooks: Chemie – eppas zum Lerna und Lehra. |
| Wikibooks: Allgemeine und Anorganische Chemie – eppas zum Lerna und Lehra. |

![{\displaystyle K={\frac {[Produkte]}{[Edukte]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/91fe9c027a16200345d4a563f5a85f409f88b5be)
![{\displaystyle K={\frac {[HI]^{2}}{[H_{2}]\cdot [I_{2}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fc2f177bb5278fdfa378fa3d4f6deadd40cd5a90)

![{\displaystyle v={\frac {-d[A]}{dt}}=k\cdot [A]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/53182a80887455faf1469476f11b5ffde8247100)

![{\displaystyle K_{S}={\frac {[A^{-}]\cdot [H_{3}O^{+}]}{[HA]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/838f3330568ce7c925cfb1d00cff0a2501446276)

![{\displaystyle K_{B}={\frac {[BH^{+}]\cdot [OH^{-}]}{[B]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/717b8d85cba4c6a006d32f12343d0faf2a86f146)

![{\displaystyle K={\frac {[OH^{-}]\cdot [H_{3}O^{+}]}{[H_{2}O]^{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c66056fe2f6008875481d7e242776919a0cb060d)
![{\displaystyle K_{w}=K\cdot [H_{2}O]^{2}=OH^{-}\cdot H_{3}O^{+}=10^{-7}\cdot 10^{-7}=10^{-14}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/031088d071d0bc0180ceaf62f1e64379c4696da4)
![{\displaystyle pH=-lg[H_{3}O^{+}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1cb57e8fcfe377f7e4d7b34e56c38b9216c87866)
![{\displaystyle pOH=-lg[OH^{-}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/312b1c3743c2aa716cdb2cc4e292f21c6bb86bab)








